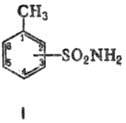
(амиды толуолсульфокислот; ф-ла I), мол. м. 171,21. Различают 2-, 3- и 4-Т., соотв. о-, М и n-Т. Все Т.-бесцв. кристаллы; для о- Т. т. пл. 158,2 °С, раств. в этаноле, ацетоне, р-римость в воде при 25 °С 0,17% по массе; для n-Т. т. пл. 137,5°С (безводный) и 105 °С (Кристаллогидрат с 2 молекулами Н 2 О), раств. в этаноле, йодном р-рё NaOH, р-римость в воде при 25 °С 0,31% по массе; для м-Т. т. пл. 108 °С.
Практич. значение имеют орто- и пара- изомеры.
Т.-слабые к-ты (для n-Т. р К а в воде 10,21); с орг. и неорг. основаниями образуют соли, при этом соли 0-Т. хуже раств. в воде, чем соли n-Т., что используют для разделения смеси изомеров. При действии сильных к-т (НС1, H2SO4) Т. гидролизуются по связи SЧN. С HNO3 незамещенные Т. образуют нитрамины, с HNO2 -толуол-сульфоновые к-ты, N-монозамещенные Т. дают N-нитрозо-производные; N-нитрозо-N-метил-n-толуолсульфамид - полупродукт для получения диазометана:
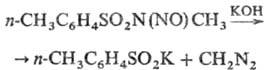
При взаимодействии n-Т. с NaClO образуется хлорамин Т, а при действии избытка хлора на щелочной р-р n-Т.-дихлорамин Т (см. Хлорамины).
В присут. к-т или оснований Т. присоединяются к изоцианатам с образованием толуолсульфонилмочевин; последние получаются также при р-ции Т. с мочевинами:
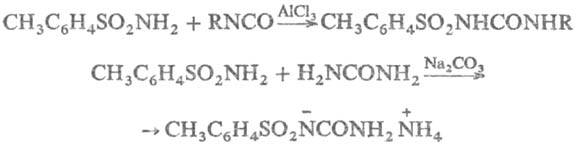
Взаимодействие Т. с сероуглеродом с послед. действием СОСl2, SOCl2 или SO2Cl2 приводит к толуолсульфонил-изотиоцианатам, напр.:
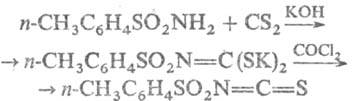
Т. конденсируются с альдегидами, напр.:
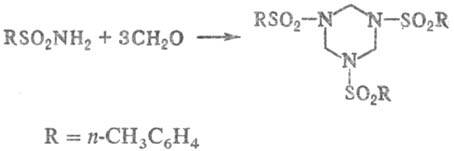
Продукты р-ции используют для получения синтетических смол.
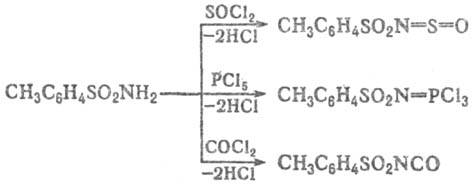
Ацилирование незамещенных и N-монозамещенных Т. протекает по атому N и приводит в зависимости от ацилирующего агента к толуолсульфонилсульфинила-минам, фосфазосоединениям, толуолсульфонилизоци-анатам либо N-ацилзамещенным толуолсульфамидам, напр.:
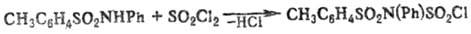
Взаимодействие n-Т. с хлорантрахиноном- способ синтеза аминоантрахинона.
Восстановит. расщепление Т. Zn в НСl, НВr или HI приводит к аминам и производным S(II); при каталитич. гидрировании, а также действии LiAlH4 Т. не восстанавливаются, за исключением N,N-дизамещенных соединений.
При окислении n-T. KМnО 4 образуется л-карбоксибензол-сульфамид HOOCC6H4SO2NH2 -полупродукт для синтеза антисептич. св-ва пантоцида, при окислении о-Т.-имид o-сульфобензоиной к-ты (сахарин).
Осн. метод получения Т.-взаимодействие толуолсульфо-хлоридов с водным р-ром NH3 (незамещенные Т.) либо с первичными или вторичными аминами (N-замещенные Т.); р-цию проводят в воде в присут. акцепторов HCl[NaOH, СаСО 3, (NH4)2CO3] либо в среде орг. р-рителей-пиридина или избытка амина.
Незамещенные Т. образуются при гидролизе толуолсуль-фонилизоцианатов либо при р-ции толуолсульфиновых к-т с гидроксиламином:
CH3C6H4SO2NCO + Н 2 О : CH3C6H4SO2NH2
n-CH3C6H4SO2H + NH2OH : n-CH3C6H4SO2NH2 + Н 2 О
N-Замещенные Т. получают алкилированием (арилирова-нием) незамещенных Т. алкил- или арилгалогенидами в щелочной среде, алкилсульфатами, алкилсульфонатами. Используют также перегруппировку N-(n-толуолсульфонил) гидразобензола в присут. сильных к-т:
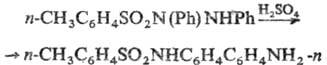
Т.-полупродукты для получения полимерных материалов, реагенты в орг. синтезе. N-Алкилтолуолсульфамиды-пластификаторы для эфиров целлюлозы.
Лит. см. при ст. Толуолсульфохлориды. Ю. Г. Шермолович.
Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988.