- ПЛАВЛЕНИЕ
-
переход в-ва из кристаллич. (твёрдого) состояния в жидкое, происходит с поглощением теплоты (фазовый переход I рода). Гл. хар-ками П. чистых в-в явл. температура плавления (Tпл) и теплота плавления (Lпл).Темп-pa П. зависит от внеш. давления р; на диаграмме состояния чистого в-ва эта зависимость изображается кривой плавления (кривой сосуществования тв. и жидкой фаз, AD или AD' на рис. 1). П. сплавов и тв. растворов происходит, как правило, в определённом интервале темп-р (исключение составляют сплавы с пост. Tпл — эвтектики).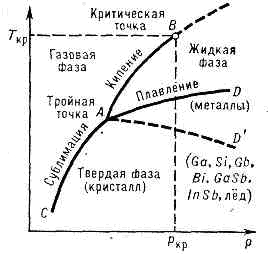 Рис. 1. Диаграмма состояния чистого в-ва (р — давление, T — темп-pa). Линии AD и AD' — кривые плавления, по линии AD' плавятся в-ва с аномальным изменением объёма при плавлении. Точка А — тройная точка; В — критич. точка.
Рис. 1. Диаграмма состояния чистого в-ва (р — давление, T — темп-pa). Линии AD и AD' — кривые плавления, по линии AD' плавятся в-ва с аномальным изменением объёма при плавлении. Точка А — тройная точка; В — критич. точка.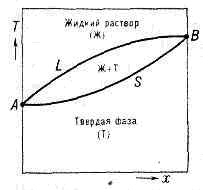 Рис. 2. Диаграмма состояния системы (напр., Cu—Ni), образующей непрерывный ряд жидких и твёрдых растворов. Жидкий раствор устойчив выше линии ликвидуса L, твёрдый — ниже линии солидуса S; между линиями L и S заключена двухфазная область равновесия твёрдых и жидких фаз.Т — темп-pa, х — состав раствора (относит. кол-во компоненты В в компоненте А).Зависимость темп-ры начала и окончания П. сплава от его состава при данном давлении изображается на диаграммах состояния спец. линиями (кривые л и к в и д у с а и с о л и д у с а, рис. 2). У ряда высокомол. соединений (напр., в-в, способных образовывать жидкие кристаллы) переход из тв. крист. состояния в изотропное жидкое происходит постадийно (в нек-ром температурном интервале), каждая стадия характеризует определённый этап разрушения крист. структуры.Наличие определённой темп-ры П.— важный признак крист. строения тв. тел. По этому признаку их легко отличить от аморфных тв. тел, к-рые не имеют фиксированной Tпл. Аморфные тв. тела переходят в жидкое состояние постепенно, размягчаясь при повышении темп-ры (см. АМОРФНОЕ СОСТОЯНИЕ).Самую высокую темп-ру П. среди чистых металлов имеет вольфрам (3410°С), самую низкую — ртуть (-38,9°С). К особо тугоплавким соединениям относятся TiN (3200°C), HfN (3580°C), ZrC (3805°C), ТаС (4070°С), HfC (4160°C) и др. Как правило, для в-в с высокой Тпл характерны более высокие значения Lпл. Примеси, присутствующие в крист. в-вах, снижают Тпл. Этим пользуются на практике для получения сплавов с низкой Тпл (напр., у т. н. сплава Вуда, состоящего из 50% Bi, 25% Pb, 12,5% Sn и 12,5% Cd, Tпл=68°С) и охлаждающих смесей (напр., смесь из льда (42,8%) и К2СО3 (57,2%) плавится при -46°С).
Рис. 2. Диаграмма состояния системы (напр., Cu—Ni), образующей непрерывный ряд жидких и твёрдых растворов. Жидкий раствор устойчив выше линии ликвидуса L, твёрдый — ниже линии солидуса S; между линиями L и S заключена двухфазная область равновесия твёрдых и жидких фаз.Т — темп-pa, х — состав раствора (относит. кол-во компоненты В в компоненте А).Зависимость темп-ры начала и окончания П. сплава от его состава при данном давлении изображается на диаграммах состояния спец. линиями (кривые л и к в и д у с а и с о л и д у с а, рис. 2). У ряда высокомол. соединений (напр., в-в, способных образовывать жидкие кристаллы) переход из тв. крист. состояния в изотропное жидкое происходит постадийно (в нек-ром температурном интервале), каждая стадия характеризует определённый этап разрушения крист. структуры.Наличие определённой темп-ры П.— важный признак крист. строения тв. тел. По этому признаку их легко отличить от аморфных тв. тел, к-рые не имеют фиксированной Tпл. Аморфные тв. тела переходят в жидкое состояние постепенно, размягчаясь при повышении темп-ры (см. АМОРФНОЕ СОСТОЯНИЕ).Самую высокую темп-ру П. среди чистых металлов имеет вольфрам (3410°С), самую низкую — ртуть (-38,9°С). К особо тугоплавким соединениям относятся TiN (3200°C), HfN (3580°C), ZrC (3805°C), ТаС (4070°С), HfC (4160°C) и др. Как правило, для в-в с высокой Тпл характерны более высокие значения Lпл. Примеси, присутствующие в крист. в-вах, снижают Тпл. Этим пользуются на практике для получения сплавов с низкой Тпл (напр., у т. н. сплава Вуда, состоящего из 50% Bi, 25% Pb, 12,5% Sn и 12,5% Cd, Tпл=68°С) и охлаждающих смесей (напр., смесь из льда (42,8%) и К2СО3 (57,2%) плавится при -46°С).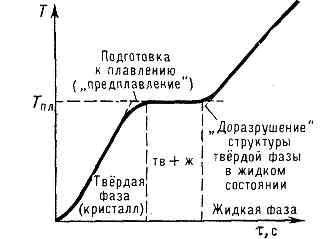 Рис. 3. Остановка изменения темп-ры при плавлении крист. тела. По оси абсцисс отложено время t, пропорциональное равномерно подводимому к телу кол-ву теплоты.П. начинается при достижении крист. в-вом Тпл и протекает при пост. темп-ре (Тпл), несмотря на сообщение в-ву теплоты (рис. 3).
Рис. 3. Остановка изменения темп-ры при плавлении крист. тела. По оси абсцисс отложено время t, пропорциональное равномерно подводимому к телу кол-ву теплоты.П. начинается при достижении крист. в-вом Тпл и протекает при пост. темп-ре (Тпл), несмотря на сообщение в-ву теплоты (рис. 3).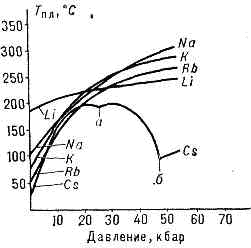 Рис. 4. Изменение темп-ры плавления Тпл (°С) щелочных металлов с увеличением давления р (кбар). Изломы на кривой плавления Cs указывают на существование у него при высоких давлениях двух полиморфных превращений (а и б).Нагреть кристалл до Т>Тпл в обычных условиях не удаётся (см. ПЕРЕГРЕВ), тогда как при кристаллизации сравнительно легко достигается значит. переохлаждение расплава.Хар-р зависимости Тпл от давления р определяется направлением объёмных изменений (DVпл) при П. (см. КЛАПЕЙРОНА — КЛАУЗИУСА УРАВНЕНИЕ). В большинстве случаев П. в-в сопровождается увеличением их объёма (обычно на неск. %). Если это имеет место, то возрастание давления приводит к повышению Тпл (рис. 4). Однако у нек-рых в-в (см. рис. 1) при П. происходит уменьшение объёма. Темп-ра П. этих в-в при увеличении давления снижается.П. сопровождается изменением физ. св-в в-ва: увеличением энтропии, что отражает разупорядочение крист. структуры; ростом теплоёмкости; электрич. сопротивления (исключение составляют нек-рые полуметаллы (Bi, Sb) и полупроводники (Ge), в жидком состоянии обладающие более высокой электропроводностью). Практически до нуля падает при П. сопротивление сдвигу (в расплаве не могут распространяться поперечные упругие волны), уменьшается скорость распространения звука (продольных волн) и т. д.Согласно мол.-кинетич. представлениям, П. осуществляется след. образом. При подведении к крист. телу теплоты увеличивается энергия колебаний (амплитуда колебаний) его атомов, что приводит к повышению темп-ры тела и способствует образованию в кристалле разл. дефектов (незаполненных узлов крист. решётки — вакансий, нарушений периодичности решётки внедрившимися между её узлами атомами и др.; (см. ДЕФЕКТЫ В КРИСТАЛЛАХ). В мол. кристаллах может происходить частичное разупорядочение взаимной ориентации осей молекул, если молекулы не обладают сферич. симметрией. Постепенный рост числа дефектов и их объединение характеризуют стадию предплавления. С достижением Тпл в кристалле создаётся критич. концентрация дефектов, начинается П.— крист. решётка распадается на легкоподвижные субмикроскопич. области. Подводимая при П. теплота идёт не на нагрев тела, а на разрыв межатомных связей и разрушение дальнего порядка в кристаллах (см. ДАЛЬНИЙ И БЛИЖНИЙ ПОРЯДОК). В самих же субмикроскопич. областях ближний порядок в расположении атомов при П. существенно не меняется (координационное число расплава при Тпл в большинстве случаев остаётся тем же, что и у кристалла). Этим объясняются меньшие значения теплот плавления Lпл по сравнению с теплотами парообразования и сравнительно небольшое изменение ряда физ. свойств в-в при их П.Процесс П. играет важную роль в природе (П. снега и льда на поверхности Земли, П. минералов в её недрах и т. д.), в науке и технике (производство чистых металлов и сплавов, литьё в формы и др.).
Рис. 4. Изменение темп-ры плавления Тпл (°С) щелочных металлов с увеличением давления р (кбар). Изломы на кривой плавления Cs указывают на существование у него при высоких давлениях двух полиморфных превращений (а и б).Нагреть кристалл до Т>Тпл в обычных условиях не удаётся (см. ПЕРЕГРЕВ), тогда как при кристаллизации сравнительно легко достигается значит. переохлаждение расплава.Хар-р зависимости Тпл от давления р определяется направлением объёмных изменений (DVпл) при П. (см. КЛАПЕЙРОНА — КЛАУЗИУСА УРАВНЕНИЕ). В большинстве случаев П. в-в сопровождается увеличением их объёма (обычно на неск. %). Если это имеет место, то возрастание давления приводит к повышению Тпл (рис. 4). Однако у нек-рых в-в (см. рис. 1) при П. происходит уменьшение объёма. Темп-ра П. этих в-в при увеличении давления снижается.П. сопровождается изменением физ. св-в в-ва: увеличением энтропии, что отражает разупорядочение крист. структуры; ростом теплоёмкости; электрич. сопротивления (исключение составляют нек-рые полуметаллы (Bi, Sb) и полупроводники (Ge), в жидком состоянии обладающие более высокой электропроводностью). Практически до нуля падает при П. сопротивление сдвигу (в расплаве не могут распространяться поперечные упругие волны), уменьшается скорость распространения звука (продольных волн) и т. д.Согласно мол.-кинетич. представлениям, П. осуществляется след. образом. При подведении к крист. телу теплоты увеличивается энергия колебаний (амплитуда колебаний) его атомов, что приводит к повышению темп-ры тела и способствует образованию в кристалле разл. дефектов (незаполненных узлов крист. решётки — вакансий, нарушений периодичности решётки внедрившимися между её узлами атомами и др.; (см. ДЕФЕКТЫ В КРИСТАЛЛАХ). В мол. кристаллах может происходить частичное разупорядочение взаимной ориентации осей молекул, если молекулы не обладают сферич. симметрией. Постепенный рост числа дефектов и их объединение характеризуют стадию предплавления. С достижением Тпл в кристалле создаётся критич. концентрация дефектов, начинается П.— крист. решётка распадается на легкоподвижные субмикроскопич. области. Подводимая при П. теплота идёт не на нагрев тела, а на разрыв межатомных связей и разрушение дальнего порядка в кристаллах (см. ДАЛЬНИЙ И БЛИЖНИЙ ПОРЯДОК). В самих же субмикроскопич. областях ближний порядок в расположении атомов при П. существенно не меняется (координационное число расплава при Тпл в большинстве случаев остаётся тем же, что и у кристалла). Этим объясняются меньшие значения теплот плавления Lпл по сравнению с теплотами парообразования и сравнительно небольшое изменение ряда физ. свойств в-в при их П.Процесс П. играет важную роль в природе (П. снега и льда на поверхности Земли, П. минералов в её недрах и т. д.), в науке и технике (производство чистых металлов и сплавов, литьё в формы и др.).
Физический энциклопедический словарь. — М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1983.
- ПЛАВЛЕНИЕ
-
- переход вещества изкристаллич. твёрдого состояния в жидкое. П. происходит с поглощением теплакак фазовый переход1-го рода, оно состоит в позиционном разупорядочениисистемы: регулярное пространственное расположение атомов (молекул) сменяетсянерегулярным при незначит. изменении ср. расстояний между ними. ТемператураП. Т пл зависит от давления Р. Для двух- и многоатомныхмолекул при П. наблюдается также ориентационное разупорядочение, у нек-рыхвеществ оно предшествует П.
Линия фазового равновесия кристалл - жидкость, отвечающая равенству химических потенциалов фаз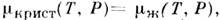 начинается в тройной точке А чистого вещества (рис. 1) и прослеживаетсядо давлений ~10ГПа. Если в системе происходит полиморфное превращение (см. Полиморфизм), толиния П. имеет излом в тройной точке кристалл I - кристалл II - жидкость. У ряда веществ с изменением темп-ры и давления наблюдается более двух полиморфныхпревращений.
начинается в тройной точке А чистого вещества (рис. 1) и прослеживаетсядо давлений ~10ГПа. Если в системе происходит полиморфное превращение (см. Полиморфизм), толиния П. имеет излом в тройной точке кристалл I - кристалл II - жидкость. У ряда веществ с изменением темп-ры и давления наблюдается более двух полиморфныхпревращений.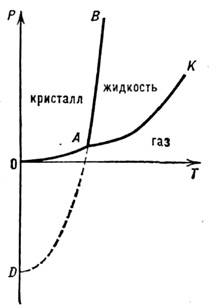
Рис. 1. Линия плавления АВ на диаграммесостояния чистого вещества: А- тройная точка равновесия кристалл- жидкость - газ, К - критическая точка, AD - экстраполяциялинии плавления за тройную точку.
Для большинства веществ темп-ра П. увеличиваетсяс ростом давления, dT пл/dP > 0. Но для воды, Ga,Bi, Sb, нек-рых сплавов dT пл/dP< 0 в окрестноститройной точки А. При плавлении энтропия S возрастает,
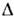 S= S ж - S крист > 0, т. е. теплота плавления .= Т
S= S ж - S крист > 0, т. е. теплота плавления .= Т 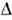 S положительна.(Известно исключение, относящееся к 3 Не при Т< 0,32К. Оно связано с явлением преимущественного ориентац. упорядочения ядерныхспинов в жидкой фазе.) Тогда, согласно Клапейрона - Клаузиуса уравнению,dP/dT =
S положительна.(Известно исключение, относящееся к 3 Не при Т< 0,32К. Оно связано с явлением преимущественного ориентац. упорядочения ядерныхспинов в жидкой фазе.) Тогда, согласно Клапейрона - Клаузиуса уравнению,dP/dT =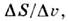 знак dP/dT совпадает со знаком скачка объёма
знак dP/dT совпадает со знаком скачка объёма 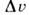 = v ж - v крист Для нормально плавящихсявеществ объём при П. увеличивается,
= v ж - v крист Для нормально плавящихсявеществ объём при П. увеличивается,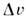 T пл при атм. давлении, приведённых значений скачков энтропии
T пл при атм. давлении, приведённых значений скачков энтропии  S/R(R - газовая постоянная )и объёма
S/R(R - газовая постоянная )и объёма 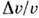 крист для нек-рых веществ.ВеществоT пл,К
крист для нек-рых веществ.ВеществоT пл,К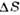 /R
/R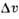 /v кристВеществоТ пл,К
/v кристВеществоТ пл,К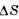 /R
/R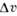 /v кристАr83,81 ,690,142Сu13581,150,046Хе161,31,710,151Аu13381,150,055N263,21 ,370,072Zn692,71,250,041O254,40,990,075А19331,360,064СН 490,71,240,081Pb600,21,000,037C6H6278,64,250,133Fe18111,010,039C6F14185,04,960,091Ni17281,230,063Na370,80,860,026NaCl10733,370,250К335,70,860,025KC110433,120,173
/v кристАr83,81 ,690,142Сu13581,150,046Хе161,31,710,151Аu13381,150,055N263,21 ,370,072Zn692,71,250,041O254,40,990,075А19331,360,064СН 490,71,240,081Pb600,21,000,037C6H6278,64,250,133Fe18111,010,039C6F14185,04,960,091Ni17281,230,063Na370,80,860,026NaCl10733,370,250К335,70,860,025KC110433,120,173Из табл. видно, что для простых веществ
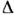 S/R лежитв интервале 0,86 - 1,71 (
S/R лежитв интервале 0,86 - 1,71 (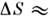 7,2 - 14,2 Дж/моль х К). Более высокие значения
7,2 - 14,2 Дж/моль х К). Более высокие значения 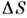 характерны для веществ, у к-рых при П. возбуждаются дополнительные (напр.,ориентацпонные) степени свободы (С 6 Н 6, C6F14 и др.) или перестраивается электронная структура (Si, Ge, Bi и др.). Увеличениеобъёма у металлов значительно меньше, чем у инертных газов и ионных солей. Зависимость Т пл элементов от их ат. номера Z немонотоннаи обнаруживает периодичность (рис. 2). Похожий вид имеет зависимость от . теплотыплавления L.
характерны для веществ, у к-рых при П. возбуждаются дополнительные (напр.,ориентацпонные) степени свободы (С 6 Н 6, C6F14 и др.) или перестраивается электронная структура (Si, Ge, Bi и др.). Увеличениеобъёма у металлов значительно меньше, чем у инертных газов и ионных солей. Зависимость Т пл элементов от их ат. номера Z немонотоннаи обнаруживает периодичность (рис. 2). Похожий вид имеет зависимость от . теплотыплавления L.
Термодинамич. движущей силой П. являетсяотклонение двухфазной системы от равновесия. Мерой этого отклонения служитразность химических потенциалов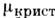 ( Т, Р)-
( Т, Р)-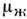 (Т, Р)>0. Стационарное состояние обеспечивается подводом тепла к границераздела фаз при постоянном внеш. давлении. П. - результат конкуренции двухфаз, каждая из к-рых устойчива по отношению к малым возмущениям..
(Т, Р)>0. Стационарное состояние обеспечивается подводом тепла к границераздела фаз при постоянном внеш. давлении. П. - результат конкуренции двухфаз, каждая из к-рых устойчива по отношению к малым возмущениям..
П. сопровождается скачкообразным изменением S,v и внутр. энергии при медленном изобарич. нагревании образца. ПриП. не только теряется регулярность структуры (дальний порядок в расположенииатомов), но существенно изменяется в среднем и координация соседних атомов(ближний порядок).
Зависимость между Т и Р налинии П. приближённо передаётся эмпирич. ур-нием ( Р/Р 0)+1 = ( Т/Т п) с. Здесь с Т 0 и Р 0 (Т п - темп-pa плавления при Р = 0, Р 0 = -Р при T= 0) получены экстраполяцией линии П. за тройную точку(ли ния АД на рис. 1). Для нормально плавящихся веществ Р0.0.
Физически продолжение линии фазового равновесияза тройную точку возможно. Обе сосуществующие фазы при этом находятся врастянутом состоянии и удовлетворяют условию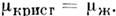 Эмпирич. ур-ние приводит к асимптотике dP/dT
Эмпирич. ур-ние приводит к асимптотике dP/dT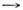 0при Т
0при Т 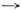 0,к-рая согласуется с теоремой Нернста. Поиск высокотемпературной асимптотикилиний П. не привёл к универсальному результату. В отличие от равновесияжидкость - пар критическая точка на линии равновесия кристалл - жидкостьне обнаружена. Её появление считается невозможным, что объясняется различиемсимметрии кристалла и жидкости.
0,к-рая согласуется с теоремой Нернста. Поиск высокотемпературной асимптотикилиний П. не привёл к универсальному результату. В отличие от равновесияжидкость - пар критическая точка на линии равновесия кристалл - жидкостьне обнаружена. Её появление считается невозможным, что объясняется различиемсимметрии кристалла и жидкости.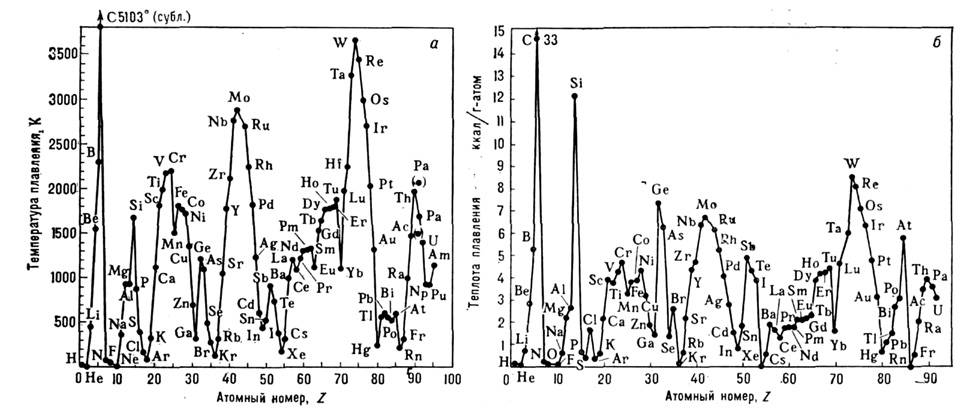
Рис. 2. Зависимость температуры ( а )и теплоты ( б) плавления элементов от их атомного номера Z.
При П. имеет место размерный эффект: темп-paП. TR малых частиц (R - эфф. радиус частицы) ниже, чем Т пл больших кристаллов. Эффект связан с поверхностнойэнергией, к-рая относительно велика для малых частиц. Напр., для Sn Т ПЛ=505 К, TR
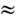 480;460; 415 К соответственно для R= 10; 6; 4 нм.
480;460; 415 К соответственно для R= 10; 6; 4 нм.
П. частично аморфных веществ, напр. полимеров, происходит в нек-ром интервале темп-р. Для двух-и многокомпонентных системравновесные составы кристаллич. и жидкой фаз различны, темп-pa П. двойногосплава зависит от его состава (концентрации х). Вид простой диаграммысостояний показан на рис. 3. Система образует непрерывный ряд растворовв жидком и кристаллич. состояниях. Равновесные составы жидкой ( х ж )и кристаллич. ( х крист) фаз при заданной темп-ре Т1 определяются, как показано на рис. 3.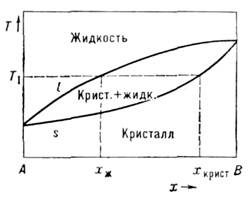
Рис. 3. Диаграмма состояния кристалл -жидкость двухкомпонентной системы, х- атомная (молекулярная) долякомпонента В в растворе.
Относит. количества фаз зависят от исходнойконцентрации однородной системы и определяются из условия сохранения масскомпонент. Верхняя линия l наз. кривой ликвидуса, нижняя линия s- кривой солидуса.
П. и кристаллизация играют важнуюроль в природе: образование снега и льда, вечной мерзлоты, процессы вовнутр. слоях Земли, вулканич. явления. П. - составная часть мн. процессовв технике (произ-во чистых металлов и сплавов, стекла, изделий из них).Лит.: Френкель Я. И., Кинетическаятеория жидкостей, Л., 1975; Любов Б. Я., Теория кристаллизации в большихобъемах, М., 1975; Тонков Е. Ю., Фазовые диаграммы элементов при высокомдавлении, М., 1979; Уббелоде А. Р., Расплавленное состояние вещества, пер. с англ., М., 1982; Скрипов В. П., Коверда В. П., Спонтанная кристаллизацияпереохлажденных жидкостей, М., 1984.
В. П. Скрипов.
Физическая энциклопедия. В 5-ти томах. — М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1988.
.