- ПОЛИМОРФИЗМ
-
(от греч. polymorphos — многообразный), способность нек-рых в-в существовать в состояниях с разл. атомно-крист. структурой (см. КРИСТАЛЛОХИМИЯ). Каждое из таких состояний (термодинамич. фаз), наз. п о л и м о р ф н о й м о д и ф и к а ц и е й, устойчиво при определённых внеш. условиях (темп-ре и давлении). Различие в структуре обусловливает и различие в св-вах полиморфных модификаций данного в-ва. П. был открыт в 1822 нем. учёным Э. Мичерлихом. Им обладают нек-рые простые в-ва (аллотропия) и мн. соединения. Так, 2 модификации углерода — кубическая (алмаз) и гексагональная (графит), резко различаются по физ. св-вам. Белое олово, имеющее тетрагональную объёмно-центрированную кристаллическую решётку,— пластичный металл, а серое олово (низкотемпературная модификация) с алмазоподобной тетрагональной решёткой — хрупкий полупроводник. Нек-рые в-ва, напр. сера и кремнезём, имеют больше чем две полимерные модификации. П. наблюдается и в жидких кристаллах.Области устойчивости полиморфных модификаций и точки перехода между ними определяются фазовыми диаграммами равновесия, расчёт к-рых основан на вычислении термодинамич. характеристик, а также спектра колебаний кристаллической решётки для разл. модификаций.Структура крист. решётки при Т=0К определяется минимумом внутр. энергии Н система ч-ц. При T>0 К структура определяется минимумом свободной энергии U куда, кроме H, входит т. н. энтропийный член SТ, связанный с тепловыми колебаниями атомов (U=H-TS, где S — энтропия). Кривая для устойчивой низкотемпературной a-фазы Ua(T) имеет вид, показанный на рис. Любой др. способ упаковки тех же атомов в кристалле (b-фаза) имеет при Т=0 К Ub>Ua..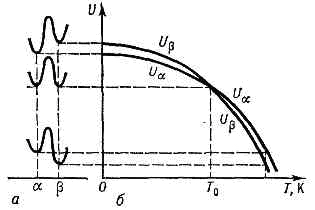 а — Изменение свободной энергии U кристалла при изменении взаимного расположения атомов; минимумы соответствуют двум устойчивым полиморфным крист. модификациям a и b; б — зависимость U от темп-ры.Это означает, что b-фаза неустойчива при низких темп-pax. Однако из-за иного характера тепловых колебаний атомов кривая Ub(T) идёт более полого, в точке Т0 она пересекается с кривой Ua и далее идёт ниже. Это означает, что при ТТ0 устойчива a-фаза, при Т>Т0 устойчива b-фаза и точка Т0 явл. точкой равновесия фаз.Переход менее стабильной модификации в более стабильную связан с преодолением энергетич. барьера, к-рый существенно меньше, если превращение происходит постепенно, путём зарождения и последоват. роста в ней областей новой фазы. Барьер преодолевается за счёт тепловых флуктуации; поэтому, если вероятность флуктуации мала, менее устойчивая фаза может длит. время существовать в метастабильном состоянии. Напр., алмаз, области существования к-рого соответствуют T>1500 К и давление р=108 Па, тем не менее может существовать неограниченно долго при атм. давлении и комнатной темп-ре, не превращаясь в стабильный при этих условиях графит. В др. веществах, наоборот, разл. модификации легко переходят друг в друга при изменении темп-ры и др.Полиморфные превращения могут сопровождаться изменением характера хим. связи и св-в. Напр., при высоких давлениях в нек-рых полупроводниках (Ge и Si) перекрытие и перестройка внеш. электронных оболочек атомов приводит к металлич. модификации. При давлении 2•1011 Па возможно возникновение металлич. водорода при 5•1010 Па — металлич. Аг, Хе.Частный случай П.— политипизм, к-рый наблюдается в нек-рых кристаллах со слоистой структурой (глинистые минералы кремния, карбид кремния и др.). Политипные модификации построены из одинаковых слоев или слоистых «пакетов» атомов и различаются способом и периодичностью наложения таких пакетов.
а — Изменение свободной энергии U кристалла при изменении взаимного расположения атомов; минимумы соответствуют двум устойчивым полиморфным крист. модификациям a и b; б — зависимость U от темп-ры.Это означает, что b-фаза неустойчива при низких темп-pax. Однако из-за иного характера тепловых колебаний атомов кривая Ub(T) идёт более полого, в точке Т0 она пересекается с кривой Ua и далее идёт ниже. Это означает, что при ТТ0 устойчива a-фаза, при Т>Т0 устойчива b-фаза и точка Т0 явл. точкой равновесия фаз.Переход менее стабильной модификации в более стабильную связан с преодолением энергетич. барьера, к-рый существенно меньше, если превращение происходит постепенно, путём зарождения и последоват. роста в ней областей новой фазы. Барьер преодолевается за счёт тепловых флуктуации; поэтому, если вероятность флуктуации мала, менее устойчивая фаза может длит. время существовать в метастабильном состоянии. Напр., алмаз, области существования к-рого соответствуют T>1500 К и давление р=108 Па, тем не менее может существовать неограниченно долго при атм. давлении и комнатной темп-ре, не превращаясь в стабильный при этих условиях графит. В др. веществах, наоборот, разл. модификации легко переходят друг в друга при изменении темп-ры и др.Полиморфные превращения могут сопровождаться изменением характера хим. связи и св-в. Напр., при высоких давлениях в нек-рых полупроводниках (Ge и Si) перекрытие и перестройка внеш. электронных оболочек атомов приводит к металлич. модификации. При давлении 2•1011 Па возможно возникновение металлич. водорода при 5•1010 Па — металлич. Аг, Хе.Частный случай П.— политипизм, к-рый наблюдается в нек-рых кристаллах со слоистой структурой (глинистые минералы кремния, карбид кремния и др.). Политипные модификации построены из одинаковых слоев или слоистых «пакетов» атомов и различаются способом и периодичностью наложения таких пакетов.
Физический энциклопедический словарь. — М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1983.
- ПОЛИМОРФИЗМ
-
(от греч. polymorphos - многообразный), способность нек-рых веществ существовать в состояниях с разд. атомно-кристаллич. структурой (см. Кристаллохимия). Каждое из таких состояний (термо-динамич. фаз), называемое полиморфной модификацией, устойчиво при опред. внеш. условиях (темп-ре и давлении). Различие в структуре обусловливает различие в свойствах полиморфных модификаций данного вещества. П. открыт в 1822 нем. учёным Э. Мичерлихом (Е. Mitscherlich). Им обладают нек-рые простые вещества (аллотропия) и мн. хим. соединения. Так, две модификации углерода - кубическая (алмаз )и гексагональная (графит) - резко различаются по физ. свойствам. Белое олово, имеющее тетрагональную объёмноцентрир. кристаллич. решётку,- пластичный металл, а серое олово (низкотемпературная модификация) с алмазоподобной тетрагональной решёткой - хрупкий полупроводник. Нек-рые вещества, напр. сера, кремнезём, вода, имеют больше чем две полиморфные модификации. П. наблюдается и у жидких кристаллов.
Области устойчивости полиморфных модификаций и точки перехода между ними определяются фазовыми диаграммами равновесия, расчёт к-рых основан на вычислении термодинамич. характеристик, а также спектра колебаний кристаллической решётки для разл. модификаций.
Структура кристаллич. решётки при Т =0 К определяется минимумом внутр. энергии
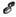 системы частиц. При
системы частиц. При 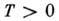 К структура определяется минимумом свободной энергии U, куда, кроме
К структура определяется минимумом свободной энергии U, куда, кроме 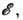 входит энтропийный член TS, связанный с тепловыми колебаниями атомов:
входит энтропийный член TS, связанный с тепловыми колебаниями атомов: 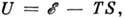 где S- энтропия. Для устойчивой низкотемпературной
где S- энтропия. Для устойчивой низкотемпературной 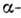 фазы зависимость U(T )имеет вид, показанный на рис. Любой др. способ упаковки тех же атомов в кристалле (
фазы зависимость U(T )имеет вид, показанный на рис. Любой др. способ упаковки тех же атомов в кристалле (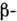 фаза) имеет при Т = О К
фаза) имеет при Т = О К 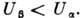 Это означает, что
Это означает, что 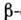 фаза неустойчива при низких темп-pax. Однако из-за иного характера тепловых колебаний атомов кривая
фаза неустойчива при низких темп-pax. Однако из-за иного характера тепловых колебаний атомов кривая 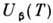 идёт более полого, в точке
идёт более полого, в точке 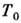 она пересекается с кривой
она пересекается с кривой 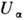 и далее идёт ниже. Это означает, что при
и далее идёт ниже. Это означает, что при 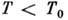 устойчива
устойчива 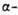 фаза, при
фаза, при 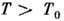 устойчива
устойчива 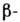 фаза, и точка
фаза, и точка 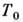 является точкой равновесия фаз.
является точкой равновесия фаз.
Фазовый переход 1-го рода менее стабильной модификации в более стабильную связан с преодолением энер-гетич. барьера, к-рый существенно меньше, если превращение происходит постепенно, путём зарождения и последоват. роста в ней областей новой фазы. Барьер преодолевается за счёт тепловых флуктуации; поэтому, если вероятность флуктуации мала, менее устойчивая фаза может длит. время существовать в метастабильном состоянии. Напр., алмаз, области стабильности к-рого соответствуют
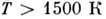 и давление
и давление 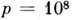 Па, тем
Па, тем не менее может существовать неограниченно долго при атм. давлении и комнатной темп-ре, не превращаясь в стабильный при этих условиях графит. В др. веществах, напр. в сегнетоэлектриках и сегнетоэластиках, наоборот, разл. модификации легко и обратимо переходят друг в друга при изменении темп-ры, давления и др., претерпевая при этом структурные фазовые переходы. В окрестности точек таких переходов физ. свойства веществ обычно экстремальны.
Частный случай П.- политипизм, к-рый наблюдается в нек-рых кристаллах со слоистой структурой (глинистые минералы кремния, карбид кремния и др.). Политипные модификации построены из одинаковых слоев или слоистых "пакетов" атомов и различаются способом и периодичностью наложения таких пакетов.
Полиморфные превращения могут сопровождаться изменением характера хим. связи и свойств. Напр., при высоких давлениях в нек-рых полупроводниках (Ge, Si) перекрытие и перестройка внеш. электронных оболочек атомов приводит к металлич. модификации. При давлении
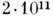 Па возможно возникновение металлического водорода, при
Па возможно возникновение металлического водорода, при 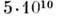 Па - металлич.
Па - металлич.Аг, Хе.
Лит.: Веrма А., Кришна П., Полиморфизм и политипизм в кристаллах, пер. с англ., М., 1969; Кристиан Д ж., Теория превращений в металлах и сплавах, пер. с англ., ч. 1, М., 1978; Уманский Я. С., Скаков Ю. А., Физика металлов, М., 1978. А. Л. Ройтбурд.
Физическая энциклопедия. В 5-ти томах. — М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1988.
.